| Beskrivning |
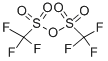
Trifluormetansulfonsyraanhydrid, även känd som triflinsyraanhydrid, har visat sig vara ett extraordinärt reagens för ett brett spektrum av transformationer. Som ett kommersiellt och lättillgängligt reagens har det använts i stor utsträckning inom syntetisk kemi på grund av dess höga elektrofilicitet. Med tanke på dess höga affinitet mot O-nukleofiler är reaktion med alkoholer, karbonyler, svavelfosfor- och jodoxider mot bildningen av motsvarande triflater starkt gynnsam. Som en av de främsta lämnande grupperna inom organisk kemi öppnar de genererade triflaterna sedan dörren till olika nedströmstransformationer, inklusive (men inte begränsat till) substitutionsreaktioner, korskopplingsprocesser, redoxreaktioner och omarrangemang[1-2] . |
| Kemiska egenskaper |
klar färglös till ljusbrun vätska |
| Används |
Trifluormetansulfonsyraanhydrid är en stark elektrofil som används i kemisk syntes för att introducera triflylgruppen. |
| Används |
Trifluormetansulfonsyraanhydrid används för att omvandla fenoler och imin till triflicester och NTf-grupp. Det är en stark elektrofil som används för introduktion av triflylgrupp i kemisk syntes. Det fungerar som ett reagens vid framställning av alkyl- och vinyltriflater och för stereoselektiv syntes av mannosazidmetyluronatdonatorer. Det fungerar som en katalysator för glykosylering med anomera hydroxisocker för att framställa polysackarider. |
| Definition |
ChEBI: Triflic-anhydrid är en organosulfonsyraanhydrid. Det är funktionellt relaterat till en triflinsyra. |
| Reaktivitetsprofil |
Elektrofil aktivering av tertiära och sekundära amider med triflinanhydrid (Tf2O; rifluormetansulfonsyraanhydrid) under milda förhållanden ger upphov till iminium- respektive iminotriflater, som skulle kunna användas som mångsidiga reagens för att reagera med olika C-, N-, O- och S -nukleofiler för omvandling av en amidfunktion till olika produkter. Andra syreinnehållande nukleofiler, såsom sulfoxider och fosforoxider, kan också genomgå nukleofila attacker med Tf2O för att generera tioniumtriflat, elektrofila P-arter och fosfoniumtriflat. Dessa mycket aktiva övergående arter kan lätt genomgå nukleofila substitutionsreaktioner för ytterligare olika transformationer. På grund av den starka elektrofila egenskapen är Tf2O dessutom benäget att reagera med relativt svaga nukleofiler såsom nitrilgrupper eller några kväveinnehållande heterocykliska föreningar. Dessutom har Tf2O också använts som ett effektivt radikaltrifluormetylerings- och trifluormetyltioleringsreagens genom frisättning av SO2 eller deoxygeneringsprocess för syntes av trifluormetylerade och trifluormetyltiolerade föreningar[2]. |
| Fara |
Kan vara frätande för metaller. Farligt vid förtäring. Orsakar allvarliga brännskador på huden och ögonskador. |
| Brandfarlighet och explosivitet |
Inte klassificerad |
| Syntes |
Syntesen av trifluormetansulfonsyraanhydrid är som följer:
En torr, {0}}ml., rundbottnad kolv laddas med 36,3 g. (0.242 mol) trifluormetansulfonsyra (not 1) och 27,3 g. (0,192 mol) fosforpentoxid (not 2). Kolven tillsluts och får stå i rumstemperatur i minst 3 timmar. Under denna period ändras reaktionsblandningen från en uppslamning till en fast massa. Kolven är försedd med ett kortvägsdestilleringshuvud och värms först med en ström av varm luft från en värmepistol och sedan med lågan från en liten brännare.Kolven värms tills trifluormetansulfonsyraanhydrid inte längre destillerar, kp 82–115 grader, vilket ger 28,4–31,2 g. (83–91%) av anhydriden, en färglös vätska. Även om denna produkt är tillräckligt ren för användning i nästa steg, kan den återstående syran avlägsnas från anhydriden genom följande procedur. En uppslamning på 3,2 g. av fosforpentoxid i 31,2 g. av den råa anhydriden omröres vid rumstemperatur i en tillsluten kolv under 18 timmar. Efter att reaktionskolven har försetts med ett kortvägsdestillationshuvud, värms den upp med ett oljebad, vilket ger 0,7 g. av förlöp, bp 74–81 grader, följt av 27,9 g. av den rena trifluormetansulfonsyraanhydriden, kp 81–84 grader .

|
| lagring |
Förvara på ett svalt, torrt, välventilerat utrymme. Fuktkänslig. |
| Reningsmetoder |
Den kan nyberedas av den vattenfria syran (11,5 g) och P2O5 (11,5 g, eller hälften av denna vikt) genom att ställa den åt sidan i rumstemperatur i 1 timme, destillera av flyktiga produkter och destillera den sedan genom en kort Vigreux-kolonn. Det hydrolyseras lätt av H2O och sönderdelas avsevärt efter några dagar för att frigöra SO2 och producera en trögflytande vätska. Förvara den torrt vid låga temperaturer. [Burdon et al. J Chem Soc 2574 1957, Beard et al. J Org Chem 38 373 1973, Beilstein 3 IV 35.] |
| Referenser |
[1] Haoqi Zhang. "Trifluormetansulfonsyraanhydrid i amidaktivering: ett kraftfullt verktyg för att skapa heterocykliska kärnor." TCIMAIL (2021).
[2] Dr. Qixue Qin, Prof. Dr. Ning Jiao, Zengrui Cheng. "Senaste tillämpningar av trifluormetansulfonsyraanhydrid i organisk syntes." Angewandte Chemie 135 10 (2022). |